Beitrag von Jörg-Michael Rupp, Präsident Interpharma, Direktor Pharma International F. Hoffmann-La Roche AG
Die forschenden pharmazeutischen Unternehmen haben in der COVID-Pandemie auf eindrückliche Art unter Beweis gestellt, was sie zum Wohle der Menschen leisten. Ermöglicht wurde dies insbesondere durch günstige Rahmenbedingungen für die Forschung. Wir als forschende Pharmaindustrie der Schweiz wollen diese Schlüsselrollen weiterhin übernehmen. Doch dafür sind wir auf entsprechende Rahmenbedingungen angewiesen.
Mit mehr als 8’000 in der Entwicklung befindlichen Arzneimitteln treibt die Pharmaindustrie die Forschung in Prävention und Patientenversorgung voran, um Menschen z.B. mit Krankheiten wie Krebs, Alzheimer, Diabetes, Infektionskrankheiten oder seltenen Krankheiten zu helfen. Insbesondere in den Bereichen Onkologie, Nervensystem und Ophtalmologika (Mittel gegen Augenerkrankungen) konnten im letzten Jahr neue aktive Substanzen in die Spezialitätenliste aufgenommen werden.
Die Pharmaindustrie hat ihre Innovationskraft insbesondere auch in der COVID-Pandemie unter Beweis gestellt. Wir sehen heute zahlreiche Diagnostika, Medikamente und Impfstoffe, die wirksam sind und dem Virus in rekordverdächtig schneller Zeit doch einiges von seinem Schrecken nehmen konnten.
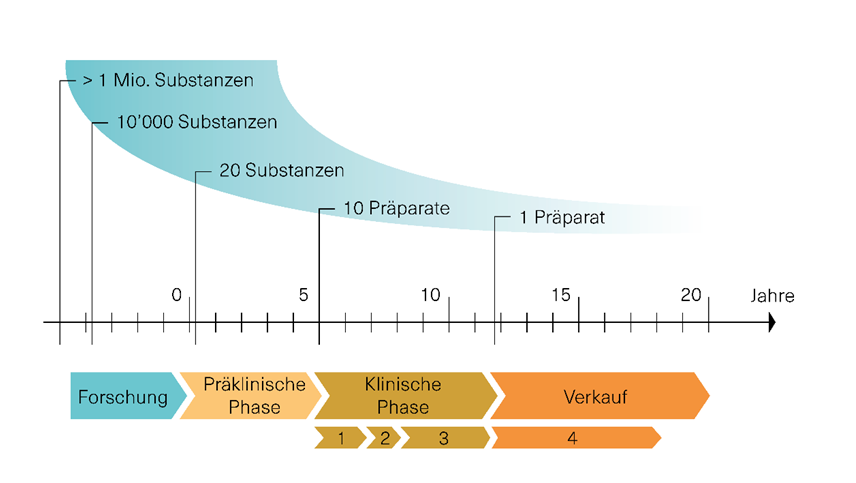
Pharmaforschung ist aber ein harter Weg. Um ein einzelnes Medikament auf den Markt zu bringen, werden 10’000 Substanzen untersucht. Davon werden nur rund zehn weiter klinisch analysiert, bis eine zu einem wirksamen Medikament entwickelt werden kann. Bis es so weit ist, sind im Durchschnitt 12 Jahre Forschung und Entwicklung notwendig. Diesen harten Weg gilt es in Kauf zu nehmen. Dabei gehören Fehlschläge in der pharmazeutischen Forschung zum Alltag: Gerade bei den Impfstoffen zeigt sich das. Von 334 COVID-Impfstoffprojekten, haben derzeit gerade erst deren 5 eine Zulassung in der EU. Zudem sind rund 600 Projekte für Medikamente oder Therapien gegen COVID-19 in der Entwicklung. In der Schweiz zugelassen sind bislang 5 dieser COVID-19 Therapeutika.
Damit Forschung erfolgreich sein kann, müssen zentrale Voraussetzungen gegeben sein. Ich möchte für die Schweiz drei Punkte herausheben:
Als erstes braucht es einen soliden Schutz des geistigen Eigentums. Das sehen wir gerade in dieser Pandemie. Patentschutz wird zwar als Problem bei der Pandemiebekämpfung wahrgenommen. Gerade der Schutz des geistigen Eigentums hat es aber den Unternehmen erlaubt, in noch nie dagewesener Form zusammenzuarbeiten und Wissen unter Forschenden zu teilen. Der Patentschutz ist in der Pandemie also Teil der Lösung, nicht Teil des Problems.
Zweitens ist für den Standort Schweiz entscheidend, ein weltweit führendes, integriertes Gesundheitsdaten-Ökosystem zu schaffen. Dafür braucht es die rechtlichen Rahmenbedingungen sowie die Zusammenarbeit von Branche, Behörden und weiteren relevanten Partnern. Hier hinken wir aber gegenüber dem Ausland massiv hinterher. Interpharma hat letztes Jahr entsprechend eine Roadmap für ein digitales Datenökosystem vorgelegt. Wir erwarten, dass die Politik nun zügig entsprechende Rahmenbedingungen setzt.
Drittens muss die Schweiz für die klinische Forschung attraktiv bleiben, um sich im internationalen Wettbewerb zu behaupten. Klinische Forschung ermöglicht Patientinnen und Patienten den Zugang zu innovativen Arzneimitteln und Behandlungsmethoden und ist essenziell für unseren Forschungsstandort. Um die Attraktivität zu fördern, müssen Bewilligungsverfahren laufend optimiert und eine beschleunigte Bewilligung für Produkte mit hohem medizinischem Bedarf eingeführt werden. Ausserdem müssen Forschungsmodelle der Zukunft wie zum Beispiel dezentrale klinische Studien und die Nutzung von Real World Data in der Schweiz rasch umsetzbar sein: Auch deshalb muss die Digitalisierung im Gesundheitswesen dringend vorankommen.
Diese drei Punkte sind aber obsolet, wenn am 13. Februar die Tier- und Menschenversuchsverbots-Initiative angenommen würde. Um es klar und deutlich zu sagen: Bei einem Ja zur Initiative gäbe es in der Schweiz keine medizinische Forschung und keinen Zugang zu medizinischen Innovationen mehr.
Die Initiative beinhaltet ein Handels- und Importverbot sämtlicher Produkte, die ganz oder teilweise unter Anwendung von Tierversuchen sowie durch Studien mit Patientinnen und Patienten entwickelt wurden. Durch die Annahme der Initiative könnten die Menschen, aber auch Tiere in der Schweiz in Zukunft von medizinischen Durchbrüchen nicht mehr profitieren, da diese in der Regel sowohl an Tieren und auch an Menschen auf ihre Wirksamkeit und Sicherheit geprüft werden müssen. Diese Überprüfung ist in den meisten Ländern vorgeschrieben – so auch in der Schweiz. Durch das vorgesehene Importverbot wäre die Schweiz über Nacht auch von sämtlichen neuen Medikamenten und innovativen Therapien aus dem Ausland abgeschnitten. Auch bisherige Produkte würden langfristig vom Markt verschwinden, denn sobald sie beispielsweise bei einer Rezeptur- oder Anwendungsänderung erneut geprüft werden müssten, dürften sie nicht mehr verkauft werden. Die medizinische Versorgung sowohl der Patientinnen und Patienten als auch der Nutz- und Haustiere würde zusammenbrechen.
Entsprechend setzt Interpharma sich stark für die Ablehnung der Tier- und Menschenversuchsverbotsinitiative durch das Stimmvolk ein. Denn diese extreme Initiative bedeutet in der Konsequenz ein Forschungsverbot in der Schweiz. Der Forschungs- und Innovationsstandort Schweiz würde zerstört und die Patientinnen und Patienten würden den Zugang zu neuen Medikamenten verlieren und damit wäre die Qualität der Gesundheitsversorgung in der Schweiz stark gefährdet.
Mehr zur Jahres-Pressekonferenz von Interpharma
 Medienmitteilung Interpharma - Themen im Jahr 2022
Medienmitteilung Interpharma - Themen im Jahr 2022
 Medienmitteilung Interpharma & vips - Medikamentenmarkt 2021
Medienmitteilung Interpharma & vips - Medikamentenmarkt 2021
Interpharma ist der Verband der forschenden pharmazeutischen Firmen der Schweiz und wurde 1933 als Verein mit Sitz in Basel gegründet.
Interpharma informiert die Öffentlichkeit über die Belange, welche für die forschende Pharmaindustrie in der Schweiz von Bedeutung sind sowie über den Pharmamarkt Schweiz, das Gesundheitswesen und die biomedizinische Forschung.
Informationen zu unseren Kennzahlen und Aktivitäten im Geschäftsjahr 2023
 mehr lesen
mehr lesen
Interpharma stellt sich vor
 mehr lesen
mehr lesen
Publikationen bestellen und herunterladen
 mehr lesen
mehr lesen
Mehr zu den Aufgaben und übergeordneten Zielen von Interpharma
 mehr lesen
mehr lesen
Setzen Sie sich mit uns in Verbindung
 mehr lesen
mehr lesen
Aktuelle Informationen und Medienkontakte für Medienschaffende
 mehr lesen
mehr lesen