L’étude d’Avenir Suisse confirme la nécessité de réformer l’accès pour les patients
Depuis 2016, le délai entre l’autorisation de mise sur le marché des médicaments et leur disponibilité effective via l’assurance-maladie est de plus en plus long. Du fait de ce décalage croissant et de l’accumulation des engorgements, les patient-e-s doivent attendre trop longtemps avant de pouvoir accéder à des médicaments très innovants. En 2022, les entreprises pharmaceutiques engagées dans la recherche ont présenté une proposition innovante visant à résoudre ce problème, mais peu de choses ont changé depuis lors. Une étude d’Avenir Suisse confirme aujourd’hui ce constat et démontre que cette proposition mériterait un débat plus large.
Pour que les médicaments et les traitements apportent un bénéfice maximal aux patient-e-s et à la société, il est essentiel que l’ensemble des patient-e-s aient rapidement accès à de telles avancées médicales. Cela correspond également au souhait de la population, car selon le Moniteur de la santé 2021, près de 93% de la population souhaite un accès immédiat aux nouveaux médicaments. Or, c’est là que le bât blesse terriblement: dans la réalité, les patient-e-s suisses doivent aujourd’hui attendre parfois plusieurs mois, voire plusieurs années, avant que ces médicaments innovants ne soient inscrits sur la liste des spécialités (LS) et donc remboursés de plein droit par l’assurance de base obligatoire – alors même que l’efficacité et la sécurité de ces médicaments ont été testées depuis longtemps par l’autorité d’autorisation Swissmedic et qu’ils ont été autorisés en raison de leur bon rapport bénéfice-risque. Ce décalage entre l’autorisation proprement dite et l’accès effectif pour les patient-e-s ne cesse de croître et un nombre toujours plus important de dossiers s’accumulent à l’Office fédéral de la santé publique (OFSP), compétent en la matière.
La Suisse a un problème d’accès aux médicaments innovants
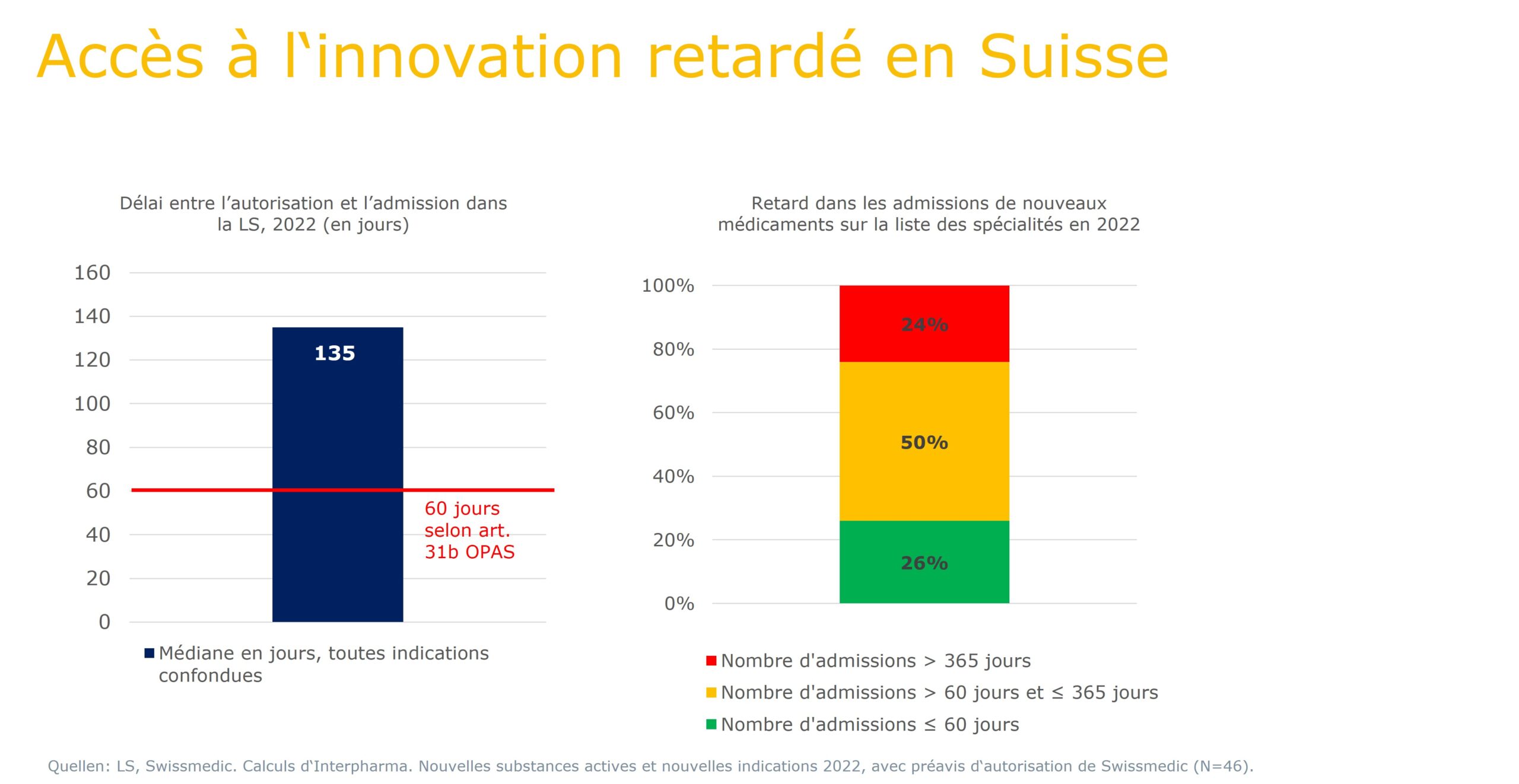
Alors qu’en 2015, il fallait en moyenne 42 jours entre l’autorisation de mise sur le marché et l’inscription sur la liste des spécialités, ce délai était en moyenne de 135 jours en 2022 – 24% des inscriptions effectuées en 2022 ont même nécessité plus de 365 jours, au lieu des 60 jours prévus par l’article 31b OPAS. De longues périodes pendant lesquelles de nombreux patient-e-s concernés doivent attendre de pouvoir accéder normalement et équitablement à des médicaments vitaux. Une situation qui peut s’avérer fatale dans les cas où le temps est compté.
Avenir Suisse demande un remboursement dès le premier jour de l’autorisation Swissmedic
Le Think Tank Avenir Suisse constate lui aussi dans une nouvelle étude (lien) la nécessité d’un mécanisme de fixation des prix plus rapide et plus simple – d’une part du point de vue des patient-e-s concerné-e-s, dont l’état de santé ne leur permet tout simplement pas d’attendre longtemps, d’autre part au vu de la logique économique selon laquelle le marché suisse, relativement petit, n’est intéressant pour les fabricants que si les conditions-cadres sont bonnes et que la bureaucratie reste limitée. Avenir Suisse critique par exemple le double rôle de l’OFSP, qui décide à la fois du prix des médicaments et des traitements de comparaison pour fixer les prix – ce qui implique un conflit d’intérêts. Par ailleurs, Avenir Suisse demande qu’à l’avenir, l’OFSP et Swissmedic examinent l’efficacité absolue et relative des nouveaux médicaments en parallèle et non pas, comme cela se fait aujourd’hui, successivement: en effet, Swissmedic examine aujourd’hui (en plus de la sécurité et de la qualité) l’efficacité absolue des médicaments. L’OFSP examine ensuite encore une fois l’efficacité de ces médicaments – mais de manière relative, c’est-à-dire en comparaison avec d’autres traitements. Avenir Suisse suggère de regrouper ces processus afin de gagner un temps précieux.
Mais Avenir Suisse estime surtout que le mécanisme de fixation des prix entre les autorités et les fabricants doit être clair et rapide afin de limiter autant que possible les retards dans l’utilisation des médicaments innovants. Cela est particulièrement important pour les médicaments très innovants, car il n’existe souvent pas d’alternatives efficaces pour les patient-e-s concerné-e-s. De plus, la procédure Fast Track de Swissmedic doit être suivie d’un processus accéléré correspondant au niveau de l’OFSP ainsi que d’une solution pour les négociations de prix entre les laboratoires pharmaceutiques et l’OFSP, qui deviennent de plus en plus complexes. Pour ce faire, l’OFSP doit inscrire les nouveaux médicaments sur la liste des spécialités à un prix provisoire immédiatement après l’autorisation par Swissmedic. Cela signifie que les caisses-maladie remboursent les médicaments innovants à un prix provisoire dès le premier jour de l’autorisation par Swissmedic afin que les patient-e-s puissent accéder immédiatement à ces médicaments et traitements. Ce prix provisoire devrait être fixé de manière mécanique et être basé, par exemple, sur le prix moyen demandé pour le même médicament dans d’autres pays de l’OCDE. Une fois le prix provisoire fixé, l’OFSP et le laboratoire pharmaceutique disposeraient de 365 jours pour négocier le prix définitif. Si le prix définitif est inférieur au prix provisoire, le fabricant devra rembourser la différence.
Le débat reste indispensable
Cette proposition d’Avenir Suisse ressemble fortement au concept de remboursement de l’accès des patient-e-s à l’innovation qu’Interpharma avait déjà présenté en mai 2022.
Selon Interpharma, l’étude d’Avenir Suisse est à saluer et constitue une contribution importante au débat. Elle confirme par ailleurs que la proposition formulée par la branche pharmaceutique en vue d’accélérer de toute urgence l’accès pour les patient-e-s en Suisse est intéressante et mérite un débat plus large. La branche pharmaceutique assume ses responsabilités et contribue à des soins de santé largement accessibles et de haute qualité, qui restent toutefois durablement finançables – non seulement en participant aux révisions régulières des prix, mais aussi en émettant des propositions d’amélioration du système constructives et sérieuses. Reste à espérer que les acteurs institutionnels continueront eux aussi à se prêter à ce débat et à contribuer de manière constructive à l’élaboration d’une solution acceptable pour toutes les parties prenantes – mais surtout pour les patient-e-s.
| Positionnement d’Interpharma par rapport à l’étude d’Avenir Suisse |
| Avenir Suisse analyse dans une nouvelle étude la mécanique du marché des médicaments à la croisée des intérêts des patients, de la réglementation et de l’industrie et aborde la question de savoir comment «assurer un accès rapide et finançable aux innovations coûteuses». Avenir Suisse y propose, entre autres, un nouveau modèle de financement pour les médicaments innovants. Interpharma se félicite qu’Avenir Suisse suggère d’accélérer le processus de remboursement des nouveaux médicaments innovants afin que les patient-e-s aient accès à des traitements vitaux dès la délivrance de l’autorisation de mise sur le marché par Swissmedic. En revanche, Interpharma se montre plus critique à l’égard du concept de «Quality Adjusted Life Years» (QALY) associé à des valeurs seuils rigides (= disposition à payer pour une année de vie en bonne santé), proposé par Avenir Suisse pour fixer les prix des nouveaux médicaments. Cette méthode controversée a une portée trop limitée, car elle privilégie les traitements bon marché mais moins efficaces au détriment des traitements complexes mais susceptibles de guérir les patient-e-s. Elle ne reflète pas non plus l’utilité sociale supplémentaire que revêt une innovation médicale (par exemple: un nouveau traitement permet à un patient de se rétablir complètement et de reprendre le travail plus rapidement, ce qui allège également les charges sociales en raison de la baisse des coûts dans les assurances sociales autres que l’AOS). De plus, cette méthode désavantage systématiquement les personnes atteintes de maladies ou de handicaps physiques rares et reste donc discutable d’un point de vue éthique. Enfin, dans de nombreux cas, des seuils rigides pour une année de vie vont à l’encontre du sentiment de justice sociétale dans la mesure où, dans certaines circonstances, le traitement de «maladies bénignes» pourrait être préféré au traitement d’une maladie grave. C’est pourquoi les QUALY ne devraient pas servir de base aux décisions de politique de santé en Suisse. |
Interlocuteur

Michèle Sierro
Responsable communication Suisse romande
