Blogserie zur Jahres-PK, Teil 2: Starker Pharmastandort, schneller und breiter Patientenzugang
Dr. Katrien De Vos, Vorsitzende des Executive Committee von Interpharma, Länderpräsidentin AstraZeneca Schweiz
In der Blogserie erfahren Sie, was die forschende Pharmaindustrie der Schweiz aus dem vergangenen Jahr mitnimmt – und vor allem, was im Jahr 2023 und darüber hinaus passieren muss, damit der Pharmastandort Schweiz weiterhin führend bleibt und die Patientinnen und Patienten Zugang zu medizinischen Innovationen haben. In Teil 2 zeigt Katrien De Vos, Länderpräsidentin von AstraZeneca Schweiz, auf, warum ein starker Pharmastandort eine wichtige Voraussetzung für schnellen und breiten Patientenzugang in der Schweiz ist.
Aktuell geben mehr als 7’000 Arzneimittel, die sich in der Entwicklung befinden, den betroffenen Menschen viel Hoffnung. Im letzten Jahr konnten in der Schweiz insgesamt rund 40 neue aktive Substanzen, schwerpunktmässig in den Bereichen Onkologie, Nervensystem oder Herz-Kreislauf in die Spezialitätenliste aufgenommen werden. Zudem helfen über 30 neu in die SL aufgenommene Indikationen beispielsweise Patientinnen und Patienten mit Krebserkrankungen sowie Stoffwechsel, Nerven- oder Infektionskrankheiten.
Doch wir müssen uns bewusst sein: Pharmaforschung ist ein riskantes Unterfangen. Die Entwicklung eines Medikamentes dauert im Schnitt 12 Jahre und das Ausfallrisiko beträgt über 90%. Von 1 Million in Frage kommender Substanzen gelangt am Ende des Innovationsprozesses schliesslich nur 1 Präparat in den Verkauf. Die mittleren Entwicklungskosten für ein innovatives Medikament betragen heute rund 2.5 Mrd. Franken – Tendenz steigend. Man muss sich vor Augen halten, dass die wenigen Medikamente, die den ganzen Weg vom Labor bis zur erfolgreichen Zulassung schaffen, auch die zahlreichen Misserfolge finanzieren müssen. Das ermöglicht uns erst, die nötigen Investitionen in Forschung und Entwicklung der Innovationen von morgen zu tätigen.
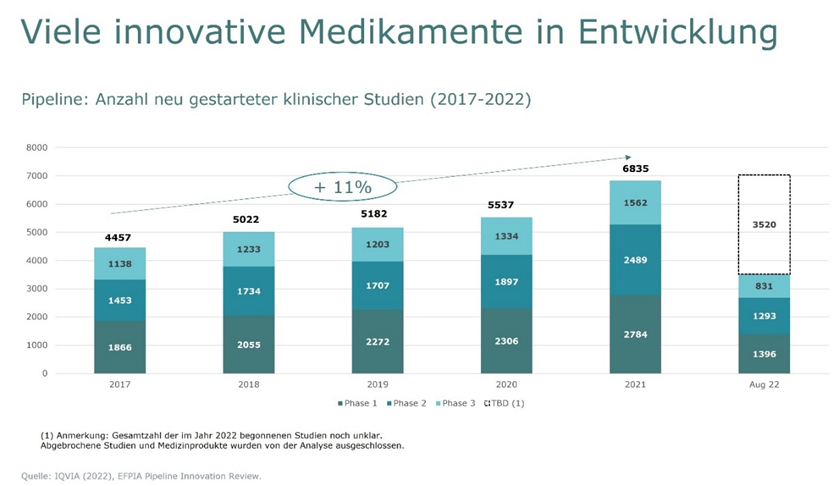
Innovative Medikamente können Gesundheitskosten senken
Abgesehen von den Entwicklungskosten ist aber auch wichtig zu verstehen, wie sich pharmazeutische Innovationen auf die Kosten des Gesundheitswesens auswirken.
Wir sehen aktuell Krankenhäuser, die in diesen Wochen an ihre Kapazitätsgrenzen gestoßen sind. In vielen Fällen fehlt es an Personal. Dabei können innovative Arzneimittel dazu beitragen, die Belastung der Krankenhäuser und die Krankheitslast für die Gesellschaft zu verringern, wie eine aktuelle Studie der Columbia University (Lichtenberg 2022) zeigt: Demnach haben pharmazeutische Innovationen zwischen 1994-2010 in der Schweiz die frühzeitige Mortalität bei unter 85-Jährigen beispielsweise um etwa ein Drittel reduziert und die Hospitalisierungen im Jahr 2019 um 2 Millionen Tage gesenkt. 2 Millionen weniger Nächte im Spital entsprechen rund 3 Mrd. Franken an Kosteneinsparungen im Gesundheitswesen.
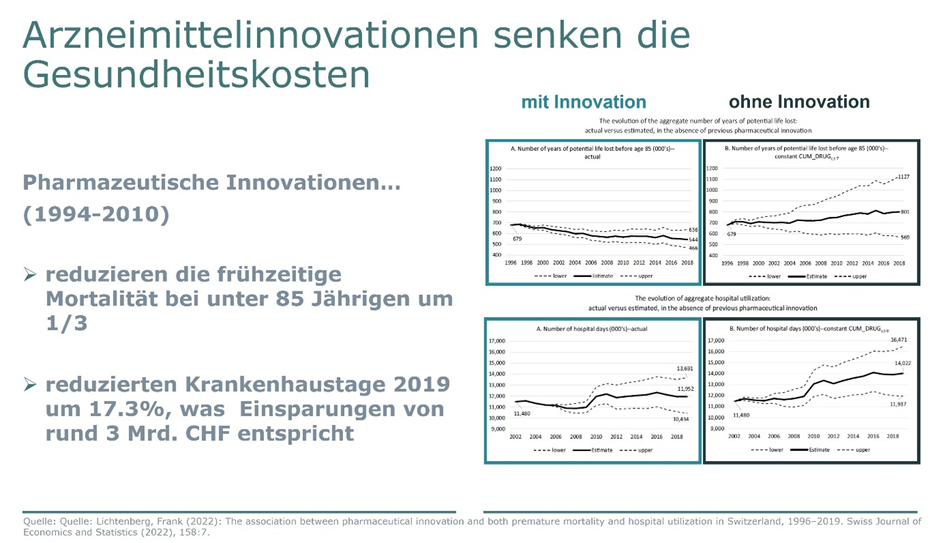
Wir sehen also, dass der Zugang zu Innovationen auch wichtig ist, um die Kostenentwicklung im Gesundheitswesen unter Kontrolle zu halten.
Patientinnen und Patienten müssen heute in der Schweiz bei innovativen Medikamenten teilweise Monate oder gar Jahre warten, bis diese auf die Spezialitätenliste und damit in die Vergütung durch die Krankenkassen genommen werden. Denn erst wenn sie auf der Spezialitätenliste stehen, haben alle Menschen in der Schweiz gleichberechtigten Zugang zu Medikamenten. Heute gelangen die innovativen und teilweise lebensrettende Therapien jedoch verzögert und rechtsungleich zu den Menschen. Daher ist es wichtig, dass in der Schweiz gute und attraktive Rahmenbedingungen für den Zugang zu neuen Medikamenten bestehen.
Dazu gehört erstens der Zulassungsprozess. Swissmedic hat den Ehrgeiz, global als eine der führenden und effizientesten Behörden wahrgenommen zu werden und jeweils unter den ersten Behörden zu sein, bei denen die Einreichung eines neuen Zulassungsgesuches erfolgt. Darin unterstützen wir als Industrie die unabhängige Zulassungsbehörde. Die Industrie steht in konstruktiv-kritischem Austausch mit Swissmedic, um die Verfahren laufend zu verbessern.
Zweitens gibt es nach wie vor auch eine Verzögerung zwischen Zulassung und der Vergütung durch die Krankenversicherungen. Diese Verzögerung betrug 2022 135 Tage und ist damit mehr als doppelt so hoch, wie es eigentlich in der Verordnung vorgesehen ist. Es ist korrekterweise festzuhalten, dass sich diese Zahl im vergangenen Jahr verbessert hat. Fakt ist aber, dass Patientinnen und Patienten in der Schweiz nach wie vor viel zu lange auf den gleichberechtigten Zugang zu neuen, innovativen Medikamenten warten müssen.
Damit die Schweiz als Markt attraktiv bleibt, ist es wichtig, dass wir gute Rahmenbedingungen haben. Auf politischer Ebene laufen jedoch Bestrebungen, die diese Attraktivität ernsthaft gefährden und damit auch den Patientenzugang in Frage stellen: Wir sprechen hier insbesondere von der Revision der Krankenversicherungs- (KVV) sowie der Krankenpflege-Leistungsverordnung (KLV), die für die Marktattraktivität und damit für die Versorgung grosse Probleme schaffen würde.

Unser Lösungsvorschlag: Der rückvergütete Innovationszugang
Wie kann diese Situation, in der wir uns derzeit befinden, gelöst werden? Wir haben im letzten Jahr einen konkreten Lösungsvorschlag entwickelt und vorgestellt: Der rückvergütete Innovationszugang garantiert den unmittelbaren Patientenzugang Das Schlüsselelement ist, dass das BAG, sobald Swissmedic die Zulassung erteilt hat, einen vorläufigen Preis festlegt und das Medikament in die Spezialitätenliste aufnimmt. Danach hat das BAG ein Jahr (statt bisher 60 Tage) Zeit, um den endgültigen Preis festzulegen. Die Differenz zwischen dem provisorischen und dem definitiven Preis wird vom Unternehmen zurückerstattet.
Dieser Vorschlag einer Rückzahlung im Gegenzug zu «Tag 0» ist aus Sicht der Industrie auch im internationalen Vergleich ein innovatives und vorteilhaftes Angebot:
- Erstens sorgt unser Vorschlag dafür, dass Patientinnen und Patienten unverzüglich Zugang zu den benötigten Arzneimitteln erhalten.
- Zweitens wird Zeit gewonnen für die Preisfindung zwischen dem BAG und den Firmen.
- Drittens besteht für die Krankenversicherung durch die Rückzahlungspflicht bzw. diese Preisgarantie kein Risiko überhöhter Preise.
- Und viertens würde diese Optimierung der Prozesse auch dafür sorgen, dass die Attraktivität des Schweizer Marktes gewahrt bleibt und die Zulassungsanträge von den Firmen möglichst früh eintreffen. Das wäre also ein grosses Plus für alle Seiten.

Entsprechend rufen wir den Bundesrat dazu auf, den Dialog und die Umsetzung des Rückvergüteten Innovationszugangs mit uns ernsthaft fortzusetzen. Unser Vorschlag kann einige grosse Probleme lösen, während die laufende KVV-Revision sie noch weiter verschärfen würde. Viele betroffene Patienten können es sich nicht leisten, jahrelang auf den Zugang zu einem lebenswichtigen Medikament zu warten.
Auch im Jahr 2023 bleibt es daher unsere oberste Priorität, uns für einen unverzüglichen und gleichberechtigten Patientenzugang zu innovativen Arzneimitteln einzusetzen. Denn hier gibt es grossen Handlungsbedarf.
Das bedeutet in der Konsequenz: Sowohl im Interesse der Patientinnen und Patienten als auch der Attraktivität des Marktes wollen wir verhindern, dass die politischen Diskussionen im Rahmen von Kostendämpfung und KVV-Revision dazu führen, dass die Versorgung mit innovativen, qualitativ hochstehenden Medikamenten aus Kostenspargründen gefährdet wird. Stattdessen unterstützen wir die Einführung von Value-based Healthcare, also einem Gesundheitswesen, welches die Optimierung von Kosten und Nutzen auf Basis von Qualitätsmessungen zum Ziel hat.
Zweitens setzen wir uns weiterhin mit Nachdruck dafür ein, dass den Patientinnen und Patienten der Zugang zu innovativen Medikamenten sofort ab dem Tag der Marktzulassung ermöglicht wird. Dafür müssen die Zulassungs- und Vergütungsprozesse weiter optimiert und modernisiert werden, zum Beispiel mit dem Vorschlag des rückvergüteten Innovationszugangs. Es ist zentral, dass wir alle uns dafür einsetzen, dass die Patientinnen und Patienten im Mittelpunkt unseres Gesundheitswesens stehen.